摘要:本文采用葡萄糖氧化酶生物传感器,利用重金属对葡萄糖氧化酶的抑制作用,来检测环境中微量的Cu2+和Hg2+浓度。以普鲁士蓝修饰的葡萄糖氧化酶电极为工作电极,饱和甘汞电极为参比电极,自制铂片电极为对电极,在三电极体系中,用循环伏安法进行扫描。考察了缓冲溶液pH值、温度等因素对葡萄糖氧化酶生物传感器检测Cu2+、Hg2+的影响。在较宽的浓度范围内,峰值电流与酶抑制剂浓度的对数呈良好的线性关系。检测Cu2+和Hg2+时,传感器的线性响应范围分别为5~40mmol/l 和2.5~22.5mmol/l,最佳响应条件选择pH值为6.86,温度为25°C。上述酶传感器可用于毒性评价和环境监测等领域。
关键词:葡萄糖氧化酶;生物传感器;重金属离子;检测
中图分类号:TP212.2 文献标识码:A
一、引言
环境监测对于环境保护非常重要,其目的是及时、准确、全面地反映环境质量现状及发展趋势,为环境管理、污染源控制、环境规划和环境评价等提供科学依据。传统的环境监测方法分析速度慢,操作复杂,所需仪器昂贵,且不适宜进行现场快速监测和连续在线分析。生物传感器具有体积小、成本低、响应快、灵敏度高、选择性及抗干扰能力强等优点,国内外对生物传感器展开了广泛深入的研究,已经研制出了葡萄糖生物传感器、乳糖生物传感器、尿酸酶生物传感器、DNA生物传感器、BOD生物传感器、测酚生物传感器等多种类别的生物传感器,来满足人们在临床检验、环境监测和生化分析[1-3]等领域中的需求。重金属在环境中存留、积累和迁移,重金属污染事件屡屡发生,给生命安全造成极大危害。重金属离子快速、有效地检测,对环境污染的防治尤其重要。
本实验将葡萄糖氧化酶固定于普鲁士蓝修饰的玻碳电极上,制成工作电极;自制铂片电极为对电极;饱和甘汞电极为参比电极;组成三电极体系,制成葡萄糖氧化酶生物传感器。待测液中的重金属抑制酶的活性,通过与葡萄糖空白液的对比,检测出该处产生的反应电流之差,然后将其换算成重金属离子浓度加以显示。利用葡萄糖氧化酶传感器检测重金属离子的浓度,是一种准确、快速、简便的方法。
二、实验部分
1、 试剂与仪器
试剂:葡萄糖氧化酶(GOD,208800units/mg, Sigma公司)、正硅酸乙酯(AR)、壳聚糖(BR)、磷酸氢二钠(AR)、磷酸二氢钾(AR)、氯化钠(AR)、实验用水为二次蒸馏水。
仪器:玻碳电极(天津兰力天仪器有限公司)、铂电极(自制,铂片长×宽×厚为5×4×0.25mm)、饱和甘汞电极(上海雷磁)、CHI600型电化学工作站(上海辰华仪器有限公司)。
2、葡萄糖氧化酶电极的制备
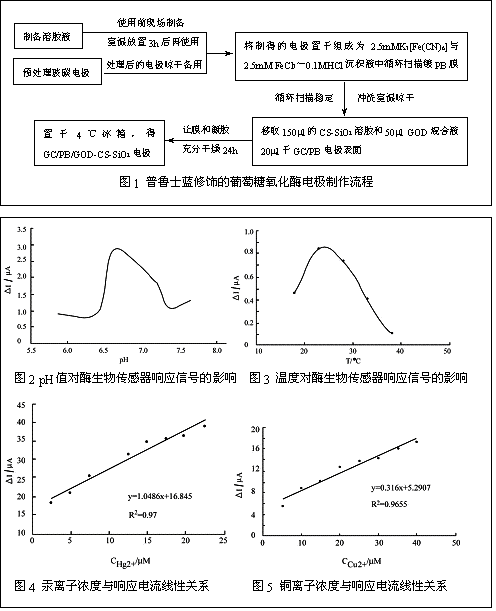
普鲁士蓝修饰的葡萄糖氧化酶电极的制备方法参考文献[4-7]。实验流程如图1所示。
3、实验方法
采用三电极体系进行检测:制作的葡萄糖氧化酶电极为工作电极,饱和甘汞电极为参比电极,自制的铂片电极为对电极,底液为0.067mol/l的磷酸盐缓冲溶液,在一定的温度下进行检测。测量时,先将三电极置于葡萄糖的缓冲溶液中,加一电压于工作电极(0.4VvsSCE),当背景电流值减小至一恒定值时,将电极放入含有一定重金属的被测溶液中,分别记录不同时间的电流响应值,扣除初始背景电流值,即为被测重金属离子浓度的电极电流响应值。
三、结果与讨论
1、缓冲溶液的pH值的影响
缓冲溶液的pH值对酶催化反应速率和酶的活性有较大影响,考查pH对酶生物传感器响应信号的影响,如图2所示。实验表明,在pH 6.86左右时出现最大电流响应。综合考虑葡萄糖氧化酶的活性以及重金属离子的响应,本实验选择pH 6.86作为最适宜的pH条件。
2、温度的影响
温度的变化将影响酶的活性及酶催化反应速率。在15~45℃范围内考察酶生物传感器与温度的关系,如上图3所示。实验表明,当温度从15°C增加到45°C时,峰电流值首先上升,在25°C时达到最大值后急剧下降。考虑到温度较高时酶容易变性失活,所以本实验选择最适宜的温度为25°C。
3、重金属离子工作曲线的测定
按所选定的最佳实验条件进行测定,电极检测汞离子和铜离子的工作曲线如图4、图5所示,在5mmol/l~40mmol/l 范围内,电极响应与汞离子的浓度成良好的线形关系;在2.5mmol/l~22.5mmol/l 范围内,电极响应与铜离子的浓度成良好的线形关系。汞离子浓度的相关系数为0.97(n=9);铜离子浓度的相关系数为0.9655(n=8)。
四、结语
本方法研制的葡萄糖氧化酶生物传感器在pH6.86,25℃时响应电流最大。检测Cu2+和Hg2+时,传感器的线性响应范围分别为5mmol/l~40mmol/l 和2.5mmol/l~22.5mmol/l ,相关系数分别为0.97和0.9655。该传感器具有操作简单、分析速度快、灵敏度高、所需试样少的特点,通过进一步研究后,有望应用于环境监测中重金属离子等潜在污染物质的检测。
参考文献:
[1] 潘涛. 生物传感器的概述和研究进展[J]. 江苏广播电视大学学报, 2002, 6(12): 55-56.
[2] Mukhopadhya K, Phadtare S, Vinod V P, et al. Gold nanoparticles assembled on amine-functionalized Na-γzeolite: A biocompatible surface for enzyme immobilization[J]. Langmurir, 2003, (19): 3858-3863.
[3] Sbrana F, Parodim T, Ricci D, et al. Langmurir films of thiolated gold nanoparticles transferred onto functionalized substrate: 2-D local organization[J]. Material Science and Engineerin C, 2002, 22(2): 187-191.
[4] 赵勤. 新型葡萄糖生物传感器及碘离子与氢离子选择性电极的研究[D]. 成都: 西南师范大学, 2003.
[5] 谭学才, 王健伟, 徐健君, 等. 固载葡萄糖氧化酶的壳聚糖二氧化硅杂化膜的制备及表征[J]. 中山大学学报, 2004, 43(4): 50-53.
[6] 黄美华, 李益恒. 分析化学中的化学修饰玻碳电极[J]. 湘潭大学学报, 2000, 24(1): 182-186.
[7] 李建平, 彭图治. 溶胶凝胶法固定胆固醇氧化酶偶联普鲁士蓝化学修饰电极的研究[J]. 高等学校化学学报, 2003, 24(5): 798-802.
Research Of Heavy Metal Ions Determination By Glucose Biosensor
Abstract: The work describes the original application of glucose biosensor to heavy metal determination. An inhibition detection scheme has been employed for detecting Hg2+ and Cu2+ by an established glucose biosensor modified by Prussian blue. Take Prussian blue modified electrode as the work electrode, the saturated calomel electrode as the reference electrode, another platinum electrode as the counter electrode. In three electrodes systems, carries on the scanning with the circulation voltammetry method. Inspected the buffer solution factor such as pH value, temperature and so on, examined the influence of Cu2+ and Hg2+ to the glucose oxidase biosensor. In a wider concentration scope, the peak value electric current and the concentration of the enzyme inhibitor assumes a good linear relationship. When examines Cu2+ and Hg2+, the linear response scope respectively is 5~40μmol/l and 2.5~22.5μmol/l. The best response condition chooses the pH6.86, 25°C. The above enzyme sensor may use in domains of toxic appraisal and environmental monitoring and so on.
Keywords: glucose oxidase; biosensor; heavy metal ions; determination
作者简介:
连兰,武汉科技大学应用化学研究所硕士研究生,研究方向为葡萄糖生物传感器。
通讯地址:武汉科技大学本部53信箱 邮编:430081。
联系电话:027-63398870 027-86536154,
E-mail:lianlan81@163.com,
伍林,武汉科技大学应用化学研究所所长,生物学博士后,从事纳米材料制备与应用及有机合成等领域的研究
易德莲,武汉科技大学副教授,主要从事有机合成及其机理的研究
秦晓蓉,武汉科技大学讲师,主要从事有机合成及生物分离
曹淑超,武汉科技大学硕士研究生,主要研究尿酸酶传感器。